
Prof. dr hab. n. med. Joanna Chorostowska-Wynimko
Kierownik Zakładu Genetyki i Immunologii Klinicznej Instytutu Gruźlicy i Chorób Płuc w Warszawie

Prof. dr hab. n. med. Dariusz M. Kowalski
Kierownik Oddziału Zachowawczego Kliniki Nowotworów Płuca i Klatki Piersiowej Narodowego Instytutu Onkologii im. Marii Skłodowskiej-Curie w Warszawie
Pacjenci z niedrobnokomórkowym rakiem płuca (NDRP) zyskali w Polsce dostęp do nowoczesnych leków immunokompetentnych. Jednak istotną kwestię stanowi odpowiednia kwalifikacja chorych do takiego leczenia.
Ludzki system odpornościowy jest bardzo inteligentny i potrafi zwalczyć wiele zagrożeń. Często pozostaje jednak bezsilny wobec nowotworu. Dzieje się tak, ponieważ komórki nowotworowe również są „inteligentne”. Potrafią radzić sobie z odpowiedzią immunologiczną naszego organizmu, który może zostać „wyłączony” w trakcie procesu nowotworowego. W rezultacie dochodzi do tzw. anergii, czyli braku reaktywności komórek odpornościowych wobec komórek raka i wygaszenia odpowiedzi obronnej. Naukowcy od dawna próbują ustalić, jak odwrócić ten proces i odnieśli już na tym polu wiele sukcesów. Do niedawna nie umieliśmy jednak wykorzystać tej wiedzy w celach terapeutycznych. W ostatnich latach nastąpił przełom. Odkryto, w jaki sposób wspomóc układ immunologiczny w walce z nowotworem „włączając” z powrotem aktywność komórek odpornościowych.
– Leki, dzięki którym osiągany jest ten efekt, określamy mianem immunokompetentnych lub immunoterapii. Leczenie polega na podaniu przeciwciał, które doprowadzają do ponownego uruchomienia naturalnej reakcji obronnej organizmu wobec wroga, jakim jest nowotwór. Jak wiadomo, wszystkie procesy wypracowane przez naturę są zazwyczaj najskuteczniejsze. Dzięki temu wśród pacjentów, których układ odpornościowy odpowiada na tego typu leczenie, uzyskujemy doskonałe efekty terapeutyczne – mówi prof. dr hab. n. med. Joanna Chorostowska-Wynimko, kierownik Zakładu Genetyki i Immunologii Klinicznej Instytutu Gruźlicy i Chorób Płuc w Warszawie.
Im szybciej – tym skuteczniej
Kluczowa jest przy tym właściwa diagnoza, ponieważ nie u każdego chorego możemy zastosować immunoterapię.
-Podstawowym narzędziem, pozwalającym zidentyfikować chorych, którzy potencjalnie odpowiedzą na to leczenie jest ocena ekspresji białka PD-L1. Jeżeli potwierdzimy, że komórki nowotworowe pozyskane drogą biopsji wykazują ekspresję tego białka w co najmniej 50 proc. komórek, to istnieje duża szansa, że immunoterapia zastosowana w pierwszej linii leczenia będzie skuteczna – tłumaczy
prof. Chorostowska-Wynimko.
Liczy się przy tym czas. Wiąże się to przede wszystkim ze stanem ogólnym chorego oraz występowaniem chorób współistniejących. Prof. Chorostowska-Wynimo podkreśla, że im szybciej zostanie zidentyfikowany problem i ustalone możliwości terapeutyczne, tym większa szansa na to, że pacjent będzie w dobrej kondycji i jego organizm lepiej zareaguje na leczenie. Drugim kryterium jest potwierdzenie, że mamy do czynienia z nowotworem, w którym nie występują tzw. wiodące zaburzenia molekularne. Czyli nie ma zmian genetycznych, które poddawałyby się terapii celowanej, czyli zastosowaniu leków ukierunkowanych molekularnie. Innymi słowy, musimy wykazać, że mamy do czynienia z nowotworem potencjalnie odpowiadającym na leczenie immunokompetentne.
Ścieżka diagnostyczna krok po kroku
Podstawowym narzędziem, którym dysponują lekarze POZ oraz sami pacjenci, jest czujność onkologiczna, czyli wrażliwość na wszelkie niepokojące objawy (tj. zmiana charakteru kaszlu, również u chorych na przewlekłe schorzenia układu oddechowego). W przypadku jakichkolwiek podejrzeń związanych z rozwojem raka płuca w pierwszej kolejności należy wykonać badanie radiologiczne (RTG) klatki piersiowej. Po wykryciu niepokojących zmian w badaniu obrazowym, chory z reguły trafia do poradni chorób płuc, gdzie diagnostyką zajmują się pulmonolodzy. Tutaj pierwszym krokiem jest najczęściej wykonanie tomografii komputerowej klatki piersiowej. Jeżeli potwierdzi ona jakieś anomalie, to dążymy do biopsji. Dzięki niej możemy pozyskać materiał do badania patomorfologicznego, które pozwala potwierdzić lub wykluczyć proces nowotworowy.
Samo potwierdzenie obecności komórek raka płuca nie wystarcza, musi zostać określony jego typ – drobnokomórkowy lub niedrobnokomórkowy. W tym ostatnim przypadku również dążymy do ustalenia podtypu: płaskonabłonkowy, gruczołowy czy też nieokreślony. W tym samym czasie należy określić stopień zaawansowania choroby, w tym obecność przerzutów. Jeżeli jest to nowotwór w stadium nieoperacyjnym, to zawsze należy rozważyć potrzebę, a raczej wykluczyć konieczność diagnostyki w kierunku biomarkerów predykcyjnych, w tym ekspresji PD-L1 i aberracji molekularnych.
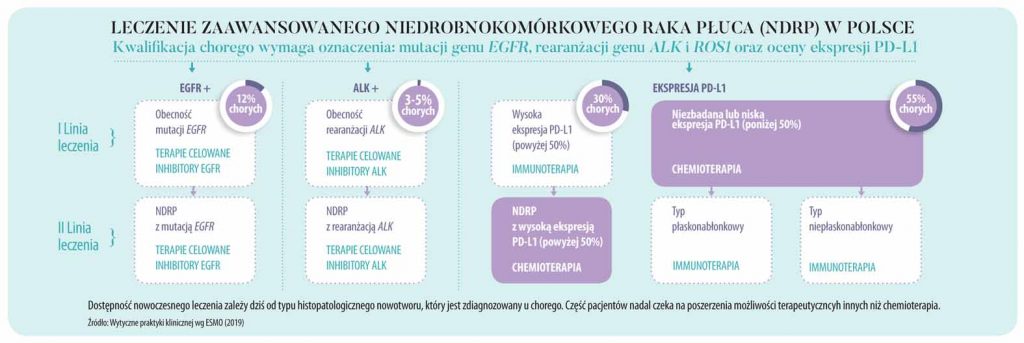
W grupie chorych z rozpoznanym rakiem gruczołowym po wykluczeniu określonych zaburzeń molekularnych, takich jak mutacja genu EGFR czy rearanżacja genów ALK i ROS1, należy zlecić oznaczenie ekspresji białka PD-L1 na powierzchni komórek nowotworowych. Od tego wyniku zależy wybór określonej opcji terapeutycznej – tłumaczy prof. dr hab. n. med. Dariusz M. Kowalski, specjalista w zakresie onkologii klinicznej i radioterapii onkologicznej, kierownik Oddziału Zachowawczego Kliniki Nowotworów Płuca i Klatki Piersiowej Narodowego Instytutu Onkologii im. Marii Skłodowskiej-Curie w Warszawie.
Nowe opcje terapeutyczne dla pacjentów z NDRP
Immunoterapia w pierwszej linii przeznaczona jest dla chorych z NDRP w stadium zaawansowanym, u których odsetek komórek nowotworowych z ekspresją PD-L1 wynosi 50 proc. lub więcej. Zastosowanie tego leczenia w formie monoterapii, zamiast klasycznej chemioterapii, skutkuje dużo lepszymi wynikami, tj. dwukrotnym wydłużeniem całkowitego czasu przeżycia przy dużo lepszej tolerancji leczenia i wyższej jakości życia – mówi prof. Kowalski.
W drugiej linii leczenia odsetek uzyskiwanej odpowiedzi jest niezależny od status PD-L1. Oznacza to, że po niepowodzeniu klasycznej chemioterapii, u pacjentów nie jest wymagane oznaczenie ekspresji PD-L1. Immunoterapia dopiero w drugiej linii powinna być jednak stosowana wyłącznie w leczeniu chorych, którzy z jakichś powodów nie mogli skorzystać z immunoterapii już w pierwszej linii.
Innowacje dostępne nie dla wszystkich
Pacjenci, dla których obecnie refundowane jest innowacyjne leczenie w pierwszej linii (tj. chorzy z mutacją w genie EGFR, rearanżacją w genach ALK lub ROS1 oraz z wysoką ekspresją PD-L1) stanowią łącznie ok. 40-45 proc. chorych z niepłaskonabłonkowym NDRP. Pozostałym chorym w Polsce pierwszej linii pozostaje praktycznie klasyczna chemioterapia.
U chorych z rakiem niepłaskonabłonkowym, głównie gruczołowym, istnieje tzw. chemioterapia dedykowana. Jest to połączenie cisplatyny lub karboplatyny z pemetreksedem (schematy dwulekowe). W raku płaskonabłonkowym – również pochodne platyny (cisplatyna lub karboplatyna, ze wskazaniem na cisplatynę) z jednym z leków tzw. drugiej generacji, tj. winorelbiną, gemcytabiną, paklitakselem. Na świecie tej grupie pacjentów, zarówno z rakiem niepłaskonabłonkowym jak i płaskonabłonkowym, jest już dedykowane leczenie skojarzone, złożone z immunoterapii w połączeniu z chemioterapią. Niestety, pomimo rejestracji w UE, tego typu postępowanie nie ma jeszcze w naszym kraju statusu refundacyjnego – stwierdza prof. Kowalski.
Konieczna jest kompleksowa opieka
U pacjentów z rakiem płuca niezwykle ważna jest przy tym ścisła współpraca wielu specjalistów, wchodzących w skład tzw. zespołu multidyscyplinarnego. Dlaczego?
Po pierwsze: rak płuca jest nowotworem trudnym diagnostycznie. Po drugie: opcje jego leczenia wykraczają poza farmakoterapię. Często poza nią w grę wchodzi zabieg operacyjny, a także radio- i chemioterapia. Ponadto chorzy są zwykle obciążeni dodatkowymi chorobami, które wymagają opieki innych specjalistów. W procesie terapeutycznym istotna jest również rehabilitacja oraz odpowiednia dieta. To wszystko sprawia, że pacjent wymaga bardzo kompleksowej opieki – tłumaczy prof. Chorostowska
POPRZEDNI
NASTĘPNY
POWIĄZANE ARTYKUŁY



